Kontrola
spalania
1. Cel ćwiczenia
Celem ćwiczenia jest oznaczenie składu spalin gazu
miejskiego przy użyciu uproszczonego aparatu Orsata i/lub automatycznego
miernika elektronicznego TESTO350, współczynnika nadmiaru powietrza l. a także obliczenie temperatury spalin t
sp
2. Podstawy
teoretyczne
W czasie spalania wyzwala się ciepło, które może być
wykorzystane do ogrzewania lub może być zamienione na pracę. Maksymalną ilość
ciepła otrzymuje się przy tzw. spalaniu całkowitym i zupełnym, to jest gdy po zakończeniu
procesu spalania brak jest nie spalonych cząstek paliwa oraz gdy powstają
niepalne tlenki, nie dające się dalej utleniać. Kontrolę procesu spalania
umożliwia analiza spalin, która między innymi daje informację, czy prawidłowy
jest nadmiar ilości powietrza dostarczonego do spalania, czy w spalinach nie
występuje tlenek węgla CO, którego
obecność świadczy o niedostatecznej ilości tlenu do spalania.
Pełna analiza spalin obejmuje oznaczenie:
- składu chemicznego spalin,
- współczynnika nadmiaru powietrza,
- temperatury spalania,
- strat ciepła uchodzącego ze spalinami do
otoczenia.
2.1. Definicje
i wzory obliczeniowe
Spalaniem nazywamy proces gwałtownego utleniania przebiegającego z efektami
cieplnymi i ewentualnie świetlnymi.
Źródłem tlenu do spalania jest najczęściej powietrze. Spalanie w tlenie lub w powietrzu
wzbogaconym w tlen powoduje wzrost temperatury spalania.
Temperaturą zapłonu nazywamy temperaturę niezbędną do rozpoczęcia spalania.
Temperatura (punkt) zapłonienia jest to temperatura, przy której zapalają się gazy
wydzielające się z podgrzanego paliwa płynnego. Właściwe zapalenie zachodzi w
wyższej temperaturze.
Składnikami palnymi paliwa są: C i H2 lub ich związki oraz S
(szkodliwa).
Składnikami niepalnymi paliwa są: O2,
N2, popiół, wilgoć.
Wartość opałowa “wop.” paliwa, jest to efekt cieplny
reakcji spalania, odniesiony do temperatury O oC tak, by para wodna
w spalinach nie uległa skropleniu.
Ciepło spalania “wsp.”paliwa , jest to ilość ciepła jaka
wydziela się przy spalaniu jednostki masy lub objętości paliwa przy jego
całkowitym i zupełnym spaleniu - jeśli wszystkie produkty wracają do
temperatury początkowej w takim stanie skupienia, w jakim znajdują się w stanie równowagi
trwałej (para wodna znajdująca się w spalinach musi ulec skropleniu i oddać
ciepło).
![]() (1)
(1)
gdzie:
|
r |
- |
ciepło parowania, |
|
w |
- |
wilgotność spalin, |
|
k |
- |
ilość wody powstała wskutek spalenia H2. |
![]() , (kJ/kg) (2)
, (kJ/kg) (2)
Rodzaje paliw:
Stałe:
węgiel kamienny, koks, węgiel brunatny.
Ciekłe:
ropa i jej produkty. Paliwa ciekłe
charakteryzują się dużą wartością opałową oraz brakiem popiołu i wilgoci
Gazowe:
gaz ziemny (zawiera zwykle ok. 90 % CH4).
Sztuczne: gaz świetlny, zwany również
gazem miejskim. (produkt odgazowania paliw stałych w retortach, polegającym na
jego ogrzewaniu bez dostępu powietrza,
gaz generatorowy. Jest to
gaz powstający w procesie niezupełnego
spalenia paliw stałych składa się głównie z CO i ewent. H2
Teoretyczne zapotrzebowanie powietrza “Lt” do spalania,
obliczone na podstawie reakcji utleniania składników paliwa:
a) dla paliwa stałego:
C + O2 ® CO2
12
kg + 32 kg ® 44 kg ![]()
H2 + 1/2 O2® H2O
2
kg + 16 kg ® 18 kg ![]()
S +
O2 ® SO2
32
kg + 32 kg ® 64 kg ![]()
![]() [kg O2/kg
paliwa] (3)
[kg O2/kg
paliwa] (3)
![]() [kg powietrza/kg
paliwa] (4)
[kg powietrza/kg
paliwa] (4)
b) dla paliwa gazowego:
H2 + 1/2 O2 ® H2O
1 m3 + 1/2 m3 ® 1m3 ![]()
CO + 1/2 O2 ® CO2
1 m3 + 1/2 m3 ® 1 m3 ![]()
CH4 + 2 O2 ® CO2 + 2 H2O
1 m3 + 2 m3 ® 1 m3 + 2 m3
![]()
Ot = 1/2 (H2
+ CO) + 2 CH4 - O2,
[m3 O2/m3 paliwa] (5)
![]() , [m3
powietrza/m3 paliwa] (6)
, [m3
powietrza/m3 paliwa] (6)
gdzie:
|
Ot |
- |
teoretyczne zapotrzebowanie tlenu do spalenia
jednostki paliwa, |
|
Lt |
- |
teoretyczne zapotrzebowanie powietrza do spalenia
jednostki paliwa. |
Współczynnik nadmiaru powietrza l:
![]() (7)
(7)
gdzie:
Lrzecz i Lteoret - odpowiednio,
rzeczywista i teoretyczna ilości powietrza do spa- lania
a) spalanie zupełne:
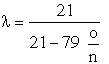 (8)
(8)
b) spalanie
niezupełne:
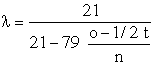 (9)
(9)
gdzie:
|
n, o, t |
- |
objętościowe udziały azotu “n”, tlenu “o” i tlenku
węgla “t” w spalinach, |
Temperatura
spalania tsp
Bilans energetyczny będący
podstawą do określenia temperatury spalania jest następujący:
![]() (10)
(10)
gdzie:
|
I2 |
- |
entalpia spalin, |
|
I1 |
- |
entalpia paliwa i powietrza do spalania. |
![]() (11)
(11)
![]() (12)
(12)
gdzie:
|
|
- |
ciepło właściwe, odpowiednio: paliwa, powietrza i
spalin, |
|
to |
- |
początkowa temperatura paliwa i powietrza. |
Po podstawieniu (11) i (12) do (10) i
przekształceniu otrzymamy:
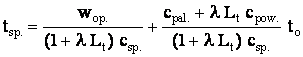 (13)
(13)
lub po uwzględnieniu, że wyrażenie przy to
zmierza do 1:
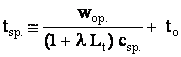 (14)
(14)
3. Analiza
spalin aparatem Orsata
Schemat stanowiska
pomiarowego przedstawia rys. 1.
Zasada oznaczania objętościowego składu spalin
opiera się na pochłanianiu CO2, CO i O2 przez odczynniki
chemiczne.
Do pochłaniania CO2 służy 33 % wodny
roztwór KOH. Pełne pochłonięcie CO2 następuje po 5-krotnym
przetłoczeniu spalin przez odczynnik.
Do pochłaniania O2 służy odczynnik o
składzie: 5 g kwasu pyrogallusowego rozpuszczonego w 15 g gorącej wodzie
destylowanej, zmieszanego następnie z 200 g 33 % wodnego roztworu KOH.
Pełna absorpcję tlenu uzyskuje się po 8-10 krotnym
przetłoczeniu próbki spalin przez odczynnik.
Do pochłaniania CO służy odczynnik zawierający
roztwór 250 g NH4Cl w 750 g wody destylowanej z dodatkiem 100 g Cu2Cl2.
Odczynnik ten szybko ulega wyczerpaniu, dlatego też najczęściej stężenie CO
oznaczamy z wykresu Ostwalda.
Uwaga! Pochłanianie składników
spalin należy prowadzić w kolejności: CO2, O2, CO.
4. Wykonanie
ćwiczenia
4.1. Przygotowanie aparatu do analizy
- wypłukane naczynia absorpcyjne napełnić
odczynnikami,
- sprawdzić szczelności połączeń w aparacie:
naczynie 7 podnieść na taką wysokość, by
ciecz w miernicy 6 osiągnęła górne, skrajne położenie. Zaworami 8 i 11 odciąć aparat od atmosfery i
spalin. Naczynie 7 opuścić, odczekać 5 minut. Jeżeli ciecz w miernicy nie opada
- układ jest szczelny,
- wyzerować poziom cieczy w miernicy 6:
ustawić naczynie 7 w swoim gnieździe. Sprawdzić
poziom cieczy w miernicy 6, jeśli menisk jest poniżej poziomu “O”- należy dolać
wody do naczynia 7, jeśli menisk jest powyżej poziomu “O” - należy z naczynia 7
odlać odpowiednią ilość cieczy.
4.2. Pobranie próbki spalin
- uruchomić palnik 1,
- przepłukać
spalinami przewody doprowadzające:
naczynie 7 podnieść na taką wysokość, by
ciecz w miernicy 6 osiągnęła górne, skrajne położenie. Zaciągnąć spaliny do
miernicy 6, ustawić zawór 11 w położenie połączenia z atmosferą, wypuścić
próbkę spalin do atmosfery przez wylot 12. Czynność powtórzyć dwukrotnie,
- zassać próbkę spalin do pomiaru:
odciąć aparat od atmosfery zaworem 12.
Naczynie 7 podnieść na taką wysokość, by ciecz w miernicy 6 osiągnęła górne,
skrajne położenie. Otworzyć połączenie z doprowadzeniem spalin zaworem 8.
Ustawić naczynie 7 w swoim gnieździe. Odciąć połączenie ze spalinami zaworem 8.
4.3. Przeprowadzenie absorpcji
4.3.1. Pochłanianie CO2
Otworzyć zawór 4 do naczynia absorpcyjnego zawierającego KOH. Za pomocą naczynia 7 przetłoczyć 5-krotnie spaliny przez odczynnik. Odstawić naczynie 7 do jej gniazda, na miernicy 6 odczytać poziom menisku.
4.3.2. Pochłanianie O2
Otworzyć zawór 5. Za pomocą
naczynia 7 przetłoczyć 8-10 krotnie spaliny przez odczynnik z kwasem
purogallusowym (czarny). Otworzyć naczynie 7 do jego gniazda, na miernicy 6
odczytać poziom menisku.
4.4. Ustalenie zawartości CO w spalinach
Z wykresu Ostwalda - rys. 2,
odczytać zawartość CO w badanej próbce spalin.
4.5. Oznaczenie współczynnika nadmiaru powietrza l
Współczynnik nadmiaru
powietrza l odczytać z wykresu Ostwalda
dla gazu miejskiego - rys. 2, oraz obliczyć ze wzoru (8) lub (9), w zależności
od tego, czy analiza wykazała obecność w spalinach CO.