TECHNIKA CIEPLNA I TERMODYNAMIKA
Ćwiczenie laboratoryjne nr 1 (6)
BADANIE PRZEMIANY IZOBARYCZNEJ
NA PRZYKLADZIE POWIETRZA WILGOTNEGO
1. Podstawowe prawa gazów
doskonałych
Podstawowe równanie stanu,
dotyczące gazów doskonałych, podał w 1834
roku C. Clapeyron. Matematyczna postać tej zależności może być zapisana w postaci:
![]() [J/kg] ( 1 )
[J/kg] ( 1 )
gdzie:
p - ciśnienie absolutne
[Pa],
v - objętość właściwa [ m3/kg],
R - indywidualna stała
gazowa [ J/(kg K)],
T - temperatura bezwzględna
[K].
Prawo to można też
przedstawić zależnością:
p1 v 1
/T 1 = p2 v2
/T 2 = R = const [ J/(kg K)]
gdzie :
p1 , p2 - ciśnienia absolutne [ Pa ],
v1 , v2 - objętości właściwe gazów
[m 3 /kg ]
Indywidualną stałą gazową
określa się na podstawie tablic lub oblicza z zależności :
R = R u / M = 8315 / M
gdzie: R u – uniwersalna stała gazowa
równa 8315 J /(kmol K),
M – masa molowa gazu , kg/ kmol
Wartość ciśnienia absolutnego jest sumą ciśnienia barometrycznego i nadciśnienia ( lub podciśnienia ) czyli wartości mierzonej manometrem (manometry mierzą tylko nadciśnienie lub podciśnienie). Do pomiaru tych wartości dla gazów wystarczają najczęściej się manometry cieczowe.
W obliczeniach
termodynamicznych, inaczej niż w zagadnieniach chemicznych, nie stosuje się
zależności wymagających znajomości masy i objętości gazu, ponieważ zwykle ich
nie znamy.
Pierwsza
zasadę termodynamiki można sformułować następująco:
Ciepło doprowadzone
z zewnątrz do nieruchomego układu
zamkniętego jest zużywane na zmianę
jego energii wewnętrznej oraz wykonanie pracy nad siłami zewnętrznymi (
pracy zewnętrznej).
Pierwszą postać pierwszej
zasady termodynamiki wyraża zależność :
dq = du + dlz = cv dT +
p dv [ J / kg ] [ 2 ]
2 )
gdzie :
dq -
elementarna zmiana ciepła [ J /
kg ],
du -
energia wewnętrzna właściwa ( dla 1 kg gazu), [ J / kg ]
du = cv dT
cv - ciepło właściwe przy stałym ciśnieniu [ J / ( kg K) ]
dlz - praca zewnętrzna dla 1 kg gazu ( równa p dv ) [
J / kg ].
Istnieje
umowa, że parametry termodynamiczne wyrażone literami małymi odnoszą się do jednostki
masy czyli do 1 kg gazu.
Druga postać
I zasady termodynamiki moze byc wyrazona :
dq = di + dlt = cp dT - v dp ( 3 )
[ 3 ]
gdzie:
di - entalpia gazu (właściwa), [
J / kg ]
dlt - praca techniczna dla 1 kg gazu, [
J / kg ]
2. Przemiana
izobaryczna
Ogólne równanie izobary, czyli przemiany
zachodzącej przy stałym ciśnieniu , ma postać :
v / T = const (
4 )
Ponieważ
różniczka stałej wartości
ciśnienia dp = 0 , z definicji
pracy technicznej mamy
dl t
= 0 [
J / kg ]
Druga postać I zasady termodynamiki może być dla przemiany izobarycznej ujęta zależnością:
d q = d i = cp dT [ J / kg ] ( 5 )
Ze
wzoru ( 5 ) wynika że ciepło przemiany
izobarycznej jest równoważne zmianie entalpii odniesionej do końca i
początku przemiany. Można to ująć zależnością
:
D q = D i = i 2 -
i 1 [ J / kg ] ( 6 )
3. Przemiana izobaryczna dla mieszaniny gazów
Do obliczeń
termodynamicznych dotyczących przemian zachodzących w mieszaninach gazów ( np.
dla powietrza wilgotnego) konieczne jest wyznaczenie średnich parametrów fizycznych
mieszaniny w oparciu o tzw. regule addytywności. Własności termofizyczne, które
stosują się do tej reguły nazywamy addytywnymi. Są to: ciepło właściwe,
entalpia, stała gazowa indywidualna i gęstość mieszaniny gazów. Jeżeli dowolny
parametr addytywny oznaczymy przez Y, to regułę addytywności można wyrazić:
![]() (1)
(1)
gdzie:
|
g1, g2, gn |
- |
udziały masowe poszczególnych składników
mieszaniny gazów. |
Poniżej podamy przykłady
wyznaczania średnich parametrów cieplnych dla przypadku powietrza wilgotnego,
traktowanego jako mieszaninę gazu suchego (azot, tlen) i pary wodnej.
Ciepło właściwe przy stałym
ciśnieniu można zapisać:
![]() (2)
(2)
gdzie:
![]() ,
,
|
X |
- |
zawartość wilgoci w powietrzu wilgotnym (w kg pary wodnej na kg gazu suchego), |
|
cgs |
- |
ciepło właściwe gazu suchego (przy stałym
ciśnieniu), |
|
cp |
- |
ciepło właściwe pary wodnej. |
Analogicznie dla stałej
gazowej mamy
![]() (3)
(3)
gdzie:
|
Rgs |
- |
stała gazowa indywidualna dla powietrza suchego, |
|
Rp |
- |
stała gazowa indywidualna dla pary wodnej |
Do wykonania obliczeń dla
powietrza wilgotnego niezbędna jest znajomość stałych gazowych i ciepeł
właściwych przy stałym ciśnieniu:
a) dla powietrza suchego odpowiednio 287 i 1005 J/(kg K) ;
b) dla pary wodnej 461
i 1930 J/ (kg K) .
Entalpia właściwa powietrza
wilgotnego igw będzie wyrażona:
![]() (4)
(4)
gdzie:
|
igs, ip |
- |
entalpie właściwe gazu (powietrza) suchego i pary
wodnej. |
Zależność (4) jest istotna
do obliczenia ciepła przemiany izobarycznej, zgodnie z zależnością:
![]() (5)
(5)
gdzie:
|
i2 |
- |
entalpia mieszaniny gazów
po przemianie, |
|
|
i1 |
- |
entalpia wlasciwa (przed
przemiana izobaryczna). |
|
Do określenia zawartości wilgoci w powietrzu stosuje się psychrometr Assmanna lub
higrometr włosowy. Związek wilgotności względnej j zawartości wilgoci X
wyraża wzór :
X = 0. 622 j ps / (pb - j ps
)
gdzie :
ps -
ciśnienie cząstkowe pary wodnej nasycającej powietrze w danej temperaturze
( maksymalna wartość przy danej temperaturze),
j
- wilgotność względna powietrza,
pb -
ciśnienie barometryczne.
Wartość ps
oblicza się dla powietrza z zależności :
ps = 1320 - 44,4 * t + 4.74 * t 2 [ Pa ]
gdzie : t
- temperatura w o C .
4. Inne parametry przemiany izobarycznej
Pracę zewnętrzną przemiany izobarycznej oblicza się z definicji :
d l = p dv
i po scałkowaniu w granicach
od v1
do v2 otrzymuje się :
l z = p ( v2 - v1 ) [ J /
kg]
Natomiast
praca techniczna przemiany izobarycznej wynika z wartości różniczki
ciśnienia: d p = 0,
czyli jest równa zeru.
Przyrost
energii wewnętrznej ( d u = c p dT ) w tej przemianie opisuje równanie :
D u = c p ( T2 - T1 ) [ J/ kg ]
5. Zagadnienia do kolokwium z tematu ” Badanie przemiany izobarycznej dla powietrza wilgotnego”
1. Pierwsza zasada termodynamiki, II postać I
zasady w ujęciu dla izobary.
2. Równanie stanu gazu, postacie ujmujące gęstość i objętość
właściwa.
3. Reguła addytywności w zastosowaniu do
obliczeń stałej gazowej, ciepła właściwego
i entalpii mieszaniny gazów
4.
Ilość ciepła wymienianego przy przemianie izobarycznej.
5.
Praca zewnętrzna dla przemiany izobarycznej
6.
Równanie i wykres przemiany izobarycznej.
7.
Równanie i wykres przemiany izotermicznej.
8.
Wyjaśnić pojęcia i podaj jednostki :
energii wewnętrznej, pracy zewnętrznej,
entalpii, entalpii właściwej i stałej
gazowej indywidualnej i uniwersalnej.
9.
Obliczanie pracy zewnętrznej i zmiany energii wewnętrznej w przemianie izobarycznej.
10. Zasada działania higrometru włosowego.
11. Pojęcia:
wilgotność względna i zawartość wilgoci.
Opracowanie sprawozdania z
tematu ” Przemiana izobaryczna”.
Sprawozdanie powinno
zawierać:
1. Opis układu pomiarowego.
2. Obliczenie zawartości wilgoci, stałej gazowej, ciepla właściwego i entalpii powietrza wilgotnego jako mieszaniny
dwuskładnikowej.
3. Określenie teoretycznej wilgotności względnej j 2 dla momentu końca przemiany izobarycznej i porównanie jej z wartością pomiarowa.
4. Obliczenie ciepła przemiany izobarycznej , pracy zewnętrznej i objętości właściwych dla początku i
końca przemiany.
5. Wykonanie wykresu izobary
w układzie pracy ( ciśnienie w funkcji objętości właściwej, p – v).
6. Wnioski.
NAZWISKO ......................... Imię ............ II rok Grupa: ..........
maj 2004
Sprawozdanie z ćwiczenia
laboratoryjnego nr (1) 7 Z = ........
„Badanie parametrów przemiany izobarycznej”
1. Dane
ogólne:
![]()
![]()
![]()
![]()
2. Obliczenie
zawartosci wilgoci 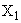 dla temperatury
dla temperatury 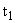
a)
cisnienie pary wodnej w
stanie nasycenia
![]() ;
; ![]()
![]() ;
; ![]()
b) ![]()
c) obliczenie
wilgotności teoretycznej dla stanu 2
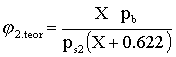
3. Obliczenie ciepła właściwego i stałej
gazowej dla powietrza wilgotnego
![]()
![]()
4.
Obliczenie
objętości właściwych
![]()
5. Obliczenie
pracy zewnętrznej
![]()
6. Obliczenie
ciepła przemiany q
![]()
7. Ciepło
właściwe przy stałej objętości
![]()
8. Przyrost
energii wewnętrznej
![]()
9. Sprawdzenie poprawności obliczeń za pomocą współczynnika
weryfikacyjnego Z
![]()
*Na odwrocie: schemat układu, wykres izobary, wnioski (j2 , j2.teor)
Alfabetyczny ciąg parametrów występujących w równaniach opisujących
procesy termodynamiczne
1. Alfabet polski:
a, cp,
cv, g, h, i, I, k, lz, lt, Lz,
Lt, m,
![]() , M, p, pb, pc, pd,
ps**, q, Q, R, Ru,
s, t, T, u, U, w, , Z
, M, p, pb, pc, pd,
ps**, q, Q, R, Ru,
s, t, T, u, U, w, , Z
2. Alfabet grecki:
r, n, v, V, c, j, x, X, ![]()
* dwa znaczenia