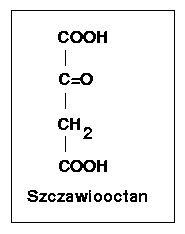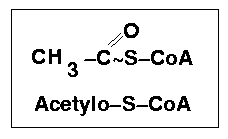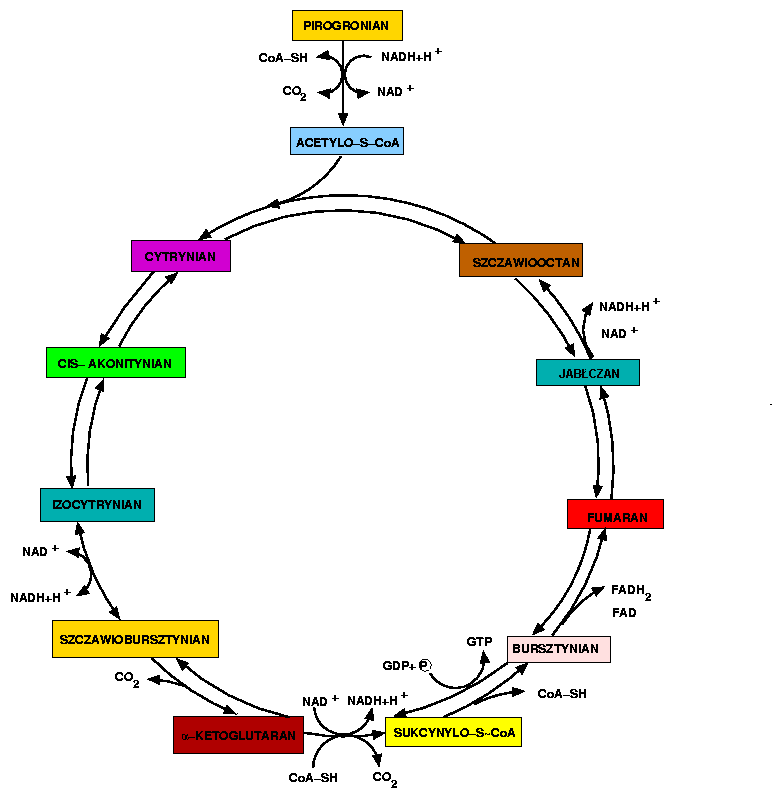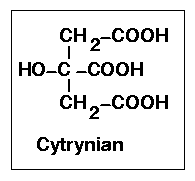
Acetylo-S-CoA wchodzi do cyklu kwasów trikarboksylowych w wyniku reakcji katalizowanej przez syntazę cytrynianową i polega na połączeniu ze szczawiooctanem. W reakcji grupa ketonowa szczawiooctanu łączy się na zasadzie kondensacji aldolowej z acetylokoenzymem A przy czym uwalnia się koenzym A. Produkt reakcji (cytrynian) może się nagromadzić w znacznych stężeniach w przypadku zahamowania działania lub syntezy następnego enzymu (np. fermentacja cytrynianowa prowadzona przez szczepy Aspergillus).
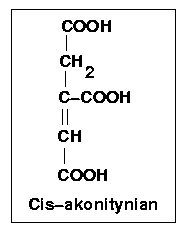
Przebiega wg panujących poglądów przez stadium cis-akonitanu i jest katalizowana przez hydratazę akonitanowa należącą do klasy liaz. W rzeczywistości produktem przejściowym między cytrynianem a izocytrynianem jest powstający, przy udziale jonu Fe3+, jon karboniowy, który pozostaje w równowadze z wymienionymi wyżej trzema kwasami trójkarboksylowymi, a więc kwas cis-akonitynowy jest produktem ubocznym przemiany.
Kilknij na strzałki aby zobaczyć szczegółowy schemat tej przemiany.
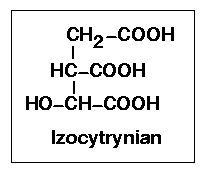
Reakcja kataizowana przez jeden z enzymów zwanych dehydrogenazami izocytrynianowymi współdziałającymi z NADP+ (fosforan dinukleotydu nikotynamidoadeninowego) lub rzadziej z NAD+ (dinukleotyd nikotynamidoadeninowy) oraz jonami Mg2+ lub Mn2+. Enzymy te katalizują przeniesienie dwóch atomów wodoru z drugorzędowej grupy alkoholowej na jeden z nukleotydów nikotynamidoadeninowych. Enzym współdziałający z NADP+ występuje w mitochondriach i frakcjach rozpuszczalnych komórki i katalizuje reakcję odwracalną. Natomiast enzym współdziałający z NAD+ występuje w mitochondriach, gdzie katalizuje reakcję nieodwracalną.
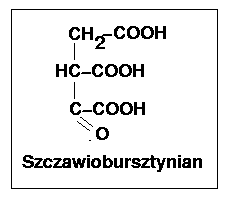
Szczawiobursztynian jest bardzo nietrwały, więc ulega natychmiastowej, jakkolwiek odwracalnej dekarboksylacji z udziałem jonu metalu, współdziałającego z tą samą dehydrogenazą (wszystko wskazuje na to iż jest to dehydrogenaza izocytrynianowa współpracująca z NADP+).
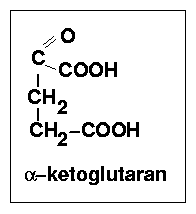
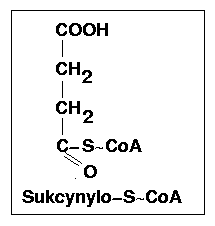
Katalizowana przez kompleksowy enzym dehydrogenazę alfa-ketoglutaranową. Jest to kompleks składajacy się z trzech odrebnych enzymów: dehydrogenazy alfa-ketoglutaranowej (dekarboksylacja alfa-ketoglutaranu do semialdehydu kwasu bursztynowego), sukcynylotransferazy dihydrolipoilowej (przeniesienie reszty semialdehydu z pirofosforanu tiaminy na kwas liponowy i utw. kwasu S-sukcynylotiooktanowego oraz przeniesienie reszty sukcynylowej z kwasu liponowego na CoA) i dehydrogenazy kwasu dihydroliponowego (odwodorowanie kwasu liponowego i ponowne utworzenie wiązania S-S) współpracującej z FAD+ i NAD+. W charakterze koenzymu dehydrogenazy alfa-ketoglutaranowej występuje pirofosforan tiaminy i jon Mg2+. Kliknij na strzałki aby zobaczyć schemat.
Reakcję tę katalizuje syntetaza sukcynylo-S-CoA. Poniewaz jednak wiązanie tioestrowe ma znaczny zasób energii, rozpad ten jest sprzężony z fosforylacją guanozynodifosforanu (GDP) do guanozynotrifosforanu (GTP) przy udziale nieorganicznego fosforanu. Jest to fosforylacja substratowa, gdyz energia potrzebna do wytworzenia makroergicznego wiązania fosforanowego jest czerpana z substratu reakcji podniesionego na wysoki poziom energetyczny. Ponieważ GTP jest w równowadze z ATP fosforylację tę można traktować jako wytworzenie cząsteczki ATP. Kliknij na strzałki aby zobaczyć schemat.
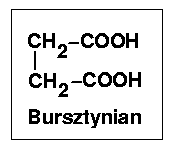
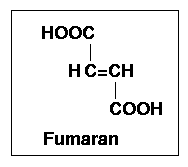
Enzymem katalizującym tę przemianę jest dehydrogenaza bursztynianowa, jest to metaloflawoproteid silnie związany z błoną mitochondrialną. Zawiera FAD i 4 atomy Fe nie związanego w hemie na mol białka, przy czym FAD jest połączony z białkiem wiązaniem peptydowm.
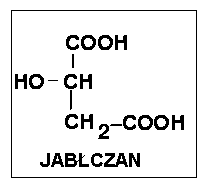
Fumaran ulega przyłączeniu cząsteczki wody, która jest katakizowana przez hydroliazę jabłczanu. Enzym ten należy do klasy liaz gdyż katalizuje odwracalne rozerwanie wiązania C-O.
Ostatni etap cyklu jest katalizowany przez dehydrogenazę jabłczanową. Enzym ten współdziała z NAD+, a przemiana pomimo, że jest odwracalna, ma równowagę znacznie przesuniętą w lewo. Utworzony szczawiooctan zamyka obrót cyklu, gdyż może zapoczątkować nową przemianę przez wejście w reakcję kondensacji z następna cząsteczką acetylo-CoA. Ponieważ reakcja kondensacji jest silnie egzoergiczna, z uwagi na udział związku o wiązaniu tioestrowym , może więc ona przesuwac równowagę poprzedzajacej reakcji w kierunku odwodorowania jabłczanu do szczawiooctanu.
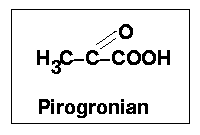
Aktywny octan tworzy się (w przypadku katabolizmu białek i cukrowców) bezpośrednio przez oksydacyjną dekarboksylację pirogronianu katalizowaną przez kompleks enzymów zwanych dehydrogenazą pirogronianową. W przypadku katabolizmu kwasów tłuszczowych acetylo-CoA tworzy się bezpośrednio przez tzw. tiolizę, czyli rozpad łańcucha beta-ketokwasu czterowęglowego acetoacetylo-CoA z udziałem grupy tiolowej koenzymu A.