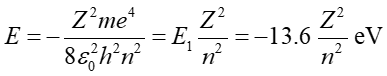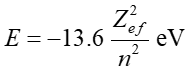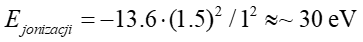36.3 Układ okresowy pierwiastków
Posługując się zasadą Pauliego można określić jakie stany w atomie są obsadzane elektronami. Skorzystamy z niej, żeby rozpatrzyć przewidywaną przez teorię kwantową strukturę niektórych pierwiastków.
Wprowadźmy do opisu konfiguracji następującą konwencję: numer powłoki
![]() (n)
piszemy cyfrą, natomiast podpowłoki
(n)
piszemy cyfrą, natomiast podpowłoki ![]() (orbitale): l = 0, 1, 2, 3, oznaczmy
literami s, p, d, f itd. (patrz paragraf 35.3). Wskaźnik górny przy symbolu podpowłoki określa liczbę
znajdujących się w niej elektronów, a wskaźnik dolny przy symbolu chemicznym pierwiastka określa wartość Z.
(orbitale): l = 0, 1, 2, 3, oznaczmy
literami s, p, d, f itd. (patrz paragraf 35.3). Wskaźnik górny przy symbolu podpowłoki określa liczbę
znajdujących się w niej elektronów, a wskaźnik dolny przy symbolu chemicznym pierwiastka określa wartość Z.
Jako pierwszy rozpatrzymy atom helu (Z = 2) → 2He: 1s2.
Najpierw przeanalizujemy zjonizowany atom He+. Jest to układ jedoelektronowy podobny do atomu wodoru, a różnica polega tylko na tym, że w jądrze helu znajdują się dwa (Z = 2) protony. W związku z tym energia takiego jonu jest dana wzorem analogicznym jak dla atomu wodoru
|
(36.4) |
a czynniki Z2 jest związany z różnicą ładunku jądra.
Jeżeli teraz dodamy drugi elektron na powłokę n = 1 to każdy z elektronów będzie
oddziaływał nie tylko z jądrem ale i z drugim elektronem; będzie się poruszał w wypadkowym polu elektrycznym
jądra (przyciąganie) i elektronu (odpychanie).
Jeżeli elektron znajduje się blisko jądra (bliżej niż drugi elektron) to porusza się w polu
kulombowskim jądra Z = 2, a jeżeli znajduje się dalej to wówczas
oddziałuje z ładunkiem jądra Z i ładunkiem drugiego elektronu
czyli porusza się w polu ładunku jądra pomniejszonego o ładunek drugiego elektronu Z − 1.
Mówimy, że elektron ekranuje ![]() ładunek jądra. Średnia arytmetyczna tych dwóch wartości daje efektywną wartość Zef = 1.5
odpowiadającą wypadkowemu ładunkowi jaki „czują” elektrony w atomie helu. Możemy więc uogólnić wzór (36.4) do postaci
ładunek jądra. Średnia arytmetyczna tych dwóch wartości daje efektywną wartość Zef = 1.5
odpowiadającą wypadkowemu ładunkowi jaki „czują” elektrony w atomie helu. Możemy więc uogólnić wzór (36.4) do postaci
|
(36.5) |
Na podstawie tak oszacowanego ładunku efektywnego otrzymujemy energię jonizacji
![]() czyli energię oderwania jednego elektronu równą około
czyli energię oderwania jednego elektronu równą około
|
W rzeczywistości elektrony nie tylko ekranują ładunek jądra ale też odpychają się nawzajem (dodatnia energia potencjalna), więc energia wiązania jest mniejsza. Zmierzona energia jonizacji helu wynosi 24.6 eV (co odpowiada Zef = 1.35).
Jest to największa energia jonizacji spośród wszystkich pierwiastków i siły chemiczne nie mogą dostarczyć takiej energii jaka jest potrzebnej do utworzenia jonu He+. Również utworzenie jonu He- jest niemożliwe bo powłoka n = 1 jest już "zapełniona" i dodatkowy elektron obsadzałby powłokę n = 2 znacznie bardziej oddaloną od jądra. Ładunek efektywny widziany przez ten elektron będzie więc równy zeru i nie działa żadna siła mogąca utrzymać ten elektron.
W rezultacie hel jest chemicznie obojętny, nie tworzy cząsteczek z żadnym pierwiastkiem. Podobnie zachowują się atomy innych pierwiastków o całkowicie wypełnionych powłokach. Nazywamy je gazami szlachetnymi.
Jako kolejny omówimy atom litu (Z = 3) → 3Li: 1s22s1.
Zgodnie z zasadą Pauliego dwa elektrony znajdują się w stanie n = 1, a trzeci elektron na powłoce n = 2. Zmierzona wartość energii jonizacji litu wynosi 5.4 eV (co odpowiada Zef = 1.25).
Taki jednokrotnie zjonizowany atom litu jest podobny do atomu helu z tą różnicą, że ze względu na ładunek jądra (Z = 3) Zef = 2.35 (jest większe o 1 niż dla helu). Oznacza to, że oderwanie drugiego elektronu wymaga energii aż 75.6 eV. Dlatego spodziewamy się, że w związkach chemicznych lit będzie wykazywać wartościowość +1.
Kolejnym pierwiastkiem jest beryl (Z = 4) → 4Be: 1s22s2.
Beryl jest podobny do litu bo zgodnie z zasadą Pauliego w stanie 2s2 mogą znajdować się dwa elektrony. Dla berylu energia oderwania (jonizacji) drugiego elektronu nie jest dużo większa niż dla pierwszego i beryl w związkach chemicznych ma wartościowość +2.
Od boru (Z = 5) do neonu (Z = 10)
bor (Z = 5) →
5B: 1s22s22p1
węgiel (Z = 6) →
6C: 1s22s22p2
azot (Z = 7) →
7N: 1s22s22p3
tlen (Z = 8) →
8O: 1s22s22p4
fluor (Z = 4) →
9F: 1s22s22p5
neon (Z = 4) →
10Ne : 1s22s22p6
W tych sześciu pierwiastkach elektrony zapełniają podpowłokę 2p (n = 2, l = 1)
Wśród tych pierwiastków na uwagę zasługują fluor i tlen, którym do zapełnienia
orbity p brakuje odpowiednio jednego i dwóch elektronów. Te
"wolne" miejsca są stanami o niskiej energii i dlatego
pierwiastki te wykazują silną tendencję do przyłączenia dodatkowych
elektronów tworząc trwałe jony Fl− i O−−. To
zjawisko jest zwane powinowactwem elektronowym
![]() .
Fluor i tlen są więc aktywnymi pierwiastkami chemicznymi.
.
Fluor i tlen są więc aktywnymi pierwiastkami chemicznymi.
Kontynuując powyższy schemat można napisać konfigurację elektronową dowolnego atomu. Okazuje się jednak, że w niektórych przypadkach przewidywane konfiguracje nie pokrywają się z obserwowanymi. Wnioskujemy, że różnice energii pomiędzy niektórymi podpowłokami muszą być tak małe, że w pewnych wypadkach może zostać odwrócona kolejność ich zapełniania. Można to zobaczyć na rysunku poniżej. Krzywe kończą się na Z = 80 (rtęć). Uwaga: skala energii nie jest liniowa.
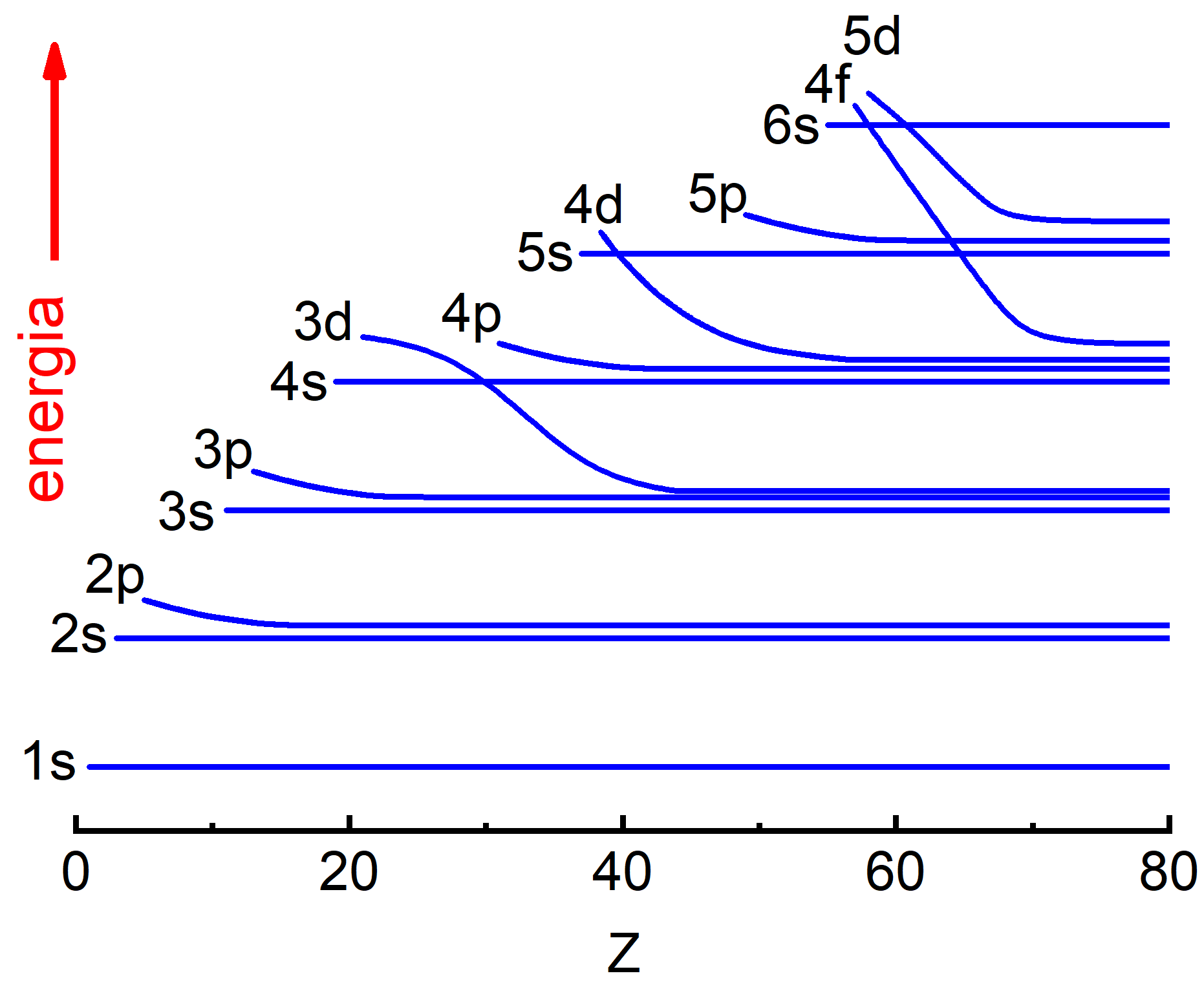
Rys. 36.4. Kolejność zapełniania podpowłok (orbitali)
Zwróćmy uwagę, że każda podpowłoka p ma wyższą energię od poprzedzającej ją powłoki s. Natomiast różnice energii pomiędzy każdą podpowłoką s i poprzedzającą ją powłoką p są szczególnie duże. W konsekwencji wzbudzenie elektronu w atomach pierwiastków, w których zakończyło się właśnie zapełnianie powłoki p jest bardzo trudne (gazy szlachetne).
W ten sposób na gruncie mechaniki kwantowej można przeanalizować własności wszystkich pierwiastków.


 Zasada Pauliego
Zasada Pauliego